研究
キーワード | 難治てんかんの病態解明と治療法の開発 | 高次脳機能と病態下の機能変容(可塑性)の解明 | 運動異常症の病態解明と治療 | 共同研究者一覧
我々は、てんかん・運動異常症の日々の臨床活動から見いだされる「臨床上の疑問」を大切にし、その解決にむけて取り組んでいます。システム神経科学の最新の知見を積極的に取り入れ、臨床てんかん学・臨床システム神経科学への還元を目指し、様々な手法を用いて研究に取り組んでいます。新学術領域「非線形発振現象を基盤としたヒューマンネイチャーの理解(オシロロジー)」「脳内身体表現の変容機構の理解と制御(身体性システム)」に参画し、様々な分野との共同研究を通じて、学際的に研究を推進しています。
キーワード
一般的なキーワード:epilepsy, epilepsy surgery, higher cortical function( motor control, praxis, language, semantic cognition, vision, will), Bereitscheftspotentials (BPs), cortico-cortical network, movement disorders, sleep disorders, autoimmune epilepsy , wideband EEG
特徴的キーワード:ictal DC shifts, cortico-cortical evoked potentials (CCEPs), cortical tremor, ictal apraxia, ictal paresis
1)難治てんかんの病態解明と治療法の開発
a)難治部分てんかんの術前評価法の開発
脳波は今尚てんかんの診断に必須であり時間分解能に優れていますが、空間分解能には制限があり皮質下構造物の評価も困難です。一方で機能的MRI(fMRI)は逆の特性を持っており、両者の同時計測(EEG-fMRI)を行うことで相補的にてんかん性放電に関連した脳領域を皮質のみならず皮質下構造物を含めて評価することが可能となってきました。我々は、本手法を用いて、てんかん発作にかかわる皮質・皮質下構造物のネットワークを明らかにし、各種てんかん病態(行為誘発性てんかん・視床下部過誤腫による症候性てんかんなど)の病態解明を試みています。難治部分てんかんの外科治療にはてんかん焦点の同定が必須ですが、近年の解剖画像の進歩で、焦点が画像で「見える」ようになり、てんかん外科の手術成績が向上してきました。しかし一方では、画像で「焦点がみえない(MRI negative)」患者では、しばしば焦点同定が困難となるため、我々は、脳磁図とEEG-fMRIを相補的に駆使することで、てんかん焦点の診断向上を目指しています。
難治部分てんかん患者の治療の選択枝として、全世界的にてんかん外科(てんかん焦点摘出術)が確立されています。手術実績が十分ある海馬硬化症による内側側頭葉てんかんや海綿状血管腫や脳腫瘍などのてんかん原性病変が「見える」症例では、一期的な焦点摘出術が可能となってきました。長時間ビデオ脳波モニタリング、解剖・機能画像検査といった非侵襲的検査で焦点が確実に同定されない症例や焦点周囲に機能野が想定される症例においては、てんかん焦点同定とその周囲の脳機能地図を作成(脳機能マッピング)するために、しばしば頭蓋内電極の慢性留置による術前評価が必要となります。京大病院では、脳神経外科・神経内科臨床神経生理グループと共同で種々の手術適応の検査を施行しています。近年のデジタル脳波計の進歩により、従来の脳波活動(0.3-70Hz)に加えて、より広範囲の脳波活動(wideband EEG)の記録が可能となり、頭蓋内電極記録においては、0.1Hz以下の緩電位(DC電位など)から300Hzを超える高周波律動までヒトの脳で可視化できるようになってきました。当施設において、頭蓋内電極から脳波記録を行った16例の難治部分てんかん患者を対象に発作時DC電位と高周波律動(HFOs)の分布・時系列、病理所見との関連を解析したところ、以下のような特徴を明らかにしました(Kanazawa et al., 2015)。
1) 発作時DC電位を16名中12症例で認め、出現頻度は発作全体の71.3%でした。
2) 発作時DC電位、HFOs、通常の発作時脳波所見の時間的関係:発作時DC 電位とHFOsをともに認めた7例中、5例ではDC電位がHFOsより統計学的有意差をもって先行していました(図1)。
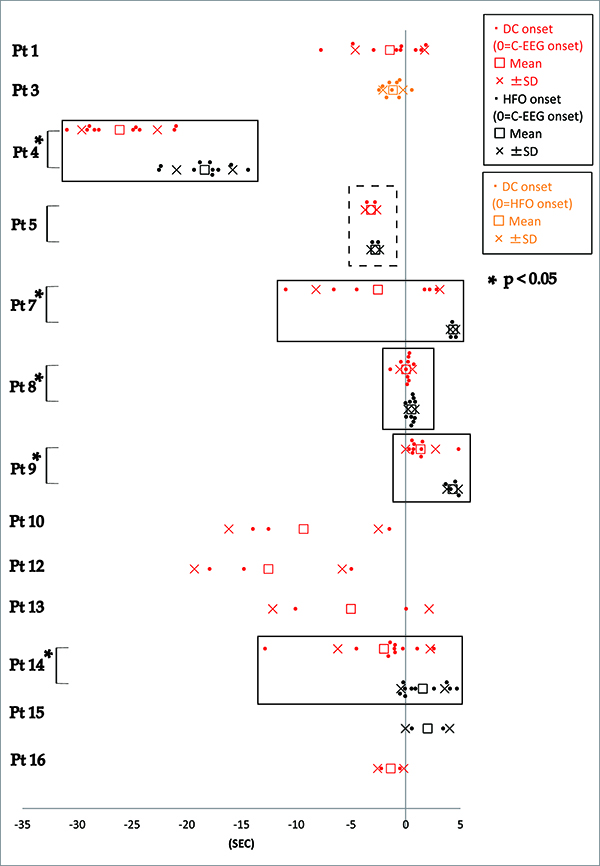 |
図1 てんかん発作時のDC電位、HFOの時系列(通常の発作時脳波変化の開始時間を0秒として表示。発作時脳波変化を認めなかった症例3ではHFOの開始時間を0秒としてDC電位の開始時間を表示。):てんかん発作時のDC電位(赤)は、高周波律動(黒)より早い傾向を示しました。そのうち5例では、統計学的有意差をもってDC電位が先行していました。Kanazawa et al., 2015より引用。 |
3) 局在性:12例(通常の発作時脳波がなかった1例、DC電位、HFOsともになかった3例を除く)では、発作時DC電位あるいはHFOsを、通常脳波より限局した範囲に認めました(平均電極数±標準偏差:通常脳波変化は16.3±17.2、発作時DC電位は9.0±11.5、HFOsは10.4±8.4電極)。1例で焦点近傍の白質内の深部電極から発作時DC電位が記録されましたが、HFOsは認められませんでした。
4) 病理所見による相違:発作時DC電位は上記の病理所見毎に①神経膠腫4例中3例(75.0%)、②皮質異形成9例中7例(77.8%)、③海馬硬化2例のうち1例(50.0%)で認められました。一方HFOsは同様に①2例(50.0%)、②4例(44.4%)、③1例(50%)で認められました。特に①のうち皮質異形成を伴う2症例における発作時DC電位、HFOsの出現率は90-100%でした。
このようなWideband EEGによる発作間欠期・発作時の超低周波(直流成分)・高周波活動(high frequency activities)の記録・解析から、従来法より感度・特異度の高いてんかん焦点同定法の確立を目指しています。
てんかん発作時発射ならびに発作間欠期のてんかん性放電は、焦点およびその周囲のみならず、焦点から皮質間ネットワークを介して遠隔領域に伝播することが経験的に知られています。このためてんかん病態の把握には、正常の皮質間ネットワークの理
解が重要です。我々は、てんかん外科の術前評価のために留置した硬膜下電極からの単発皮質電気刺激を用いて、皮質間伝播と判断される短潜時の誘発電位(皮質-皮質間誘発電位:cortico-cortical evoked potential(CCEP))を隣接・遠隔皮質から記録することにより、皮質領野間のネットワークを機能的にin vivoで調べる手法を考案し、臨床応用してきました。皮質刺激は硬膜下電極を通じて行うため1cmの空間解像度での皮質間の機能的結合の探索が可能です。本手法を用いて、てんかん焦点の単発電気刺激による焦点皮質の興奮性(てんかん原性)の評価や焦点からのてんかん性放電の伝播様式の同定に臨床応用しています。
b)各種てんかん病態の解明と治療
前述した通り、EEG-fMRIの手法により、皮質下構造物を含めて全脳を評価することが可能となってきました。我々は、本手法を用いて、行為誘発性てんかん・視床下部過誤腫(西新潟中央病院亀山茂樹先生)による症候性てんかんなどの病態解明を進めています。
近年、臨床てんかん学において自己免疫介在性の病態が明らかとなりつつあり(autoimmune epilepsy)、各種細胞膜抗体との関連が注目されています。さらに、超高磁場MRIの進歩により、このような自己免疫性脳炎でしばしば炎症の主座となる側頭葉内側(海馬・扁桃体)の微細な変化を捉えることが可能となってきました。当講座で長時間ビデオ脳波モニタリング、神経心理検査、FDG-PET、超高磁場MRIと包括的評価を行ったところ、臨床症候を伴わない脳波上の発作(subclinical seizure)が頻発し、記銘力障害が遷延することから、自己免疫介在性脳炎がくすぶり持続することを明らかにし(図2)、免疫治療介入の時期・期間などを的確に判断し治療成績向上に努めてきました(Kanazawa et al., 2014)。また、非典型な臨床像を示す症例の背景に、自己免疫性の機序が介在している場合があることを症例報告しました。短期間のうちに頭頂葉の乏突起神経膠腫・両側側頭葉の3領域にてんかん原性が示唆された症例(NMDA抗体陽性)で、薬剤に対して難治に経過、免疫療法に反応するも不十分で、頭頂葉の腫瘍切除後にてんかん発作・脳波異常ともに消失しました(Matsumoto et al., 2015)。抗LGI1抗体は、自己免疫介在性辺縁系脳炎を惹起することが知られていますが、一方でLgi1遺伝子変異によるLGI1蛋白の変化は常染色体優性外側側頭葉てんかん(ADLTE)の原因となります。両者はLGI1が病態に関わるものの、表現型は異なる点が注目されています。我々は、医学研究科附属動物実験施設との共同研究により、ADLTEのモデルとしてLgi1-L385R変異を有するヘテロラット(Lgi1L385R/+ラット)の開発を行い、さらに大阪薬科大学(大野行弘先生)と共同研究を継続しています。
内科的治療に関しては、有望な新規薬剤の治験を積極的にかつ効率よく進めています。また、本院薬剤部(矢野育子先生)との共同研究により、代謝酵素のCYP2C19の遺伝子多型の解析結果に基づいて抗てんかん薬の至適投与量あるいは効果の予測の検討をすすめています(遺伝子多型によるテーラーメード薬剤治療)。
臨床神経生理学的手法を駆使したてんかん発作治療法として、脳内電気刺激による発作抑制だけでなく、脳波変動を自己制御することで患者自身の脳活動の過度な興奮性を抑制する方法が注目されてきており、既に本施設でも良好な結果を挙げつつあります(脳波を対象としたバイオフィードバック療法)。これらの新手法の臨床応用を推進しています。
京都大学iPS細胞研究所(井上治久先生)との共同研究で、てんかんに関わるiPS細胞研究を開始しました。迷走神経刺激による発作抑制機構の解明の共同研究を行なっています(近畿大学加藤天美先生、広島大学飯田幸治先生)
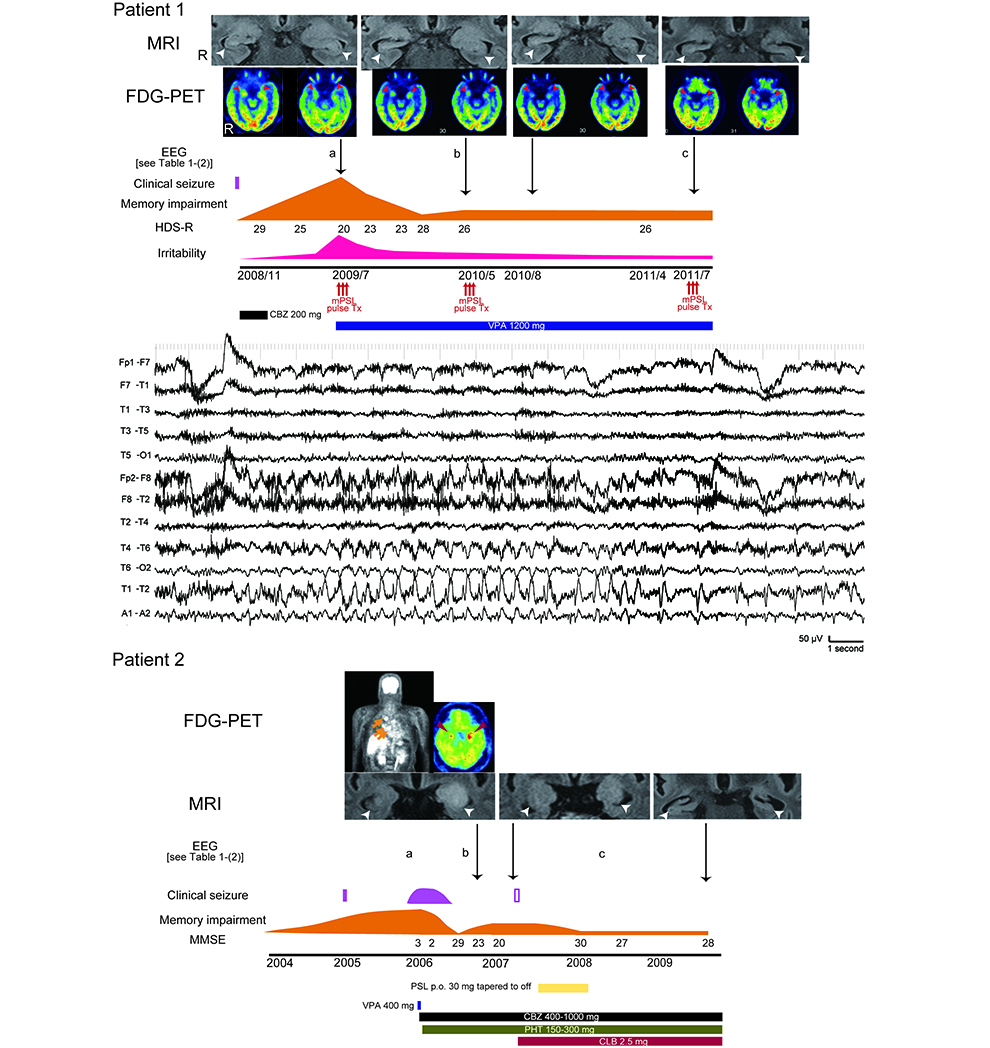
図2 自己免疫性脳炎患者(VGKC複合体抗体陽性)の1例
画像所見の推移:両側の内側側頭葉は、初期にはMRIで高信号・腫大、FDG-PETで糖代謝の亢進を示しました(矢頭)。以後、年単位で次第に内側側頭葉の萎縮を認めるようになり、糖代謝の亢進も改善しました(上段)。臨床経過:臨床症状を伴う発作は初回のみでしたが、認知機能の低下は変動・遷延しました(中段)。右側頭部の律動性放電で始まる発作時脳波変化(subclinical seizure)を認め、脳炎の病勢に一致して出現頻度が次第に減少しました(下段)。Kanazawa et al., 2014より引用。
c)脳波解析研究
生理学的検査としての臨床脳波には80年の歴史があり、てんかんのみならず、脳死を含めた意識障害、脳機能評価に必須の検査として位置づけられています。柴崎浩先生(京都大学名誉教授)が30年来継続された佐賀大学(中村政俊先生、杉剛直先生)、福岡工業大学(西田茂人先生)、札幌医科大学(長峯隆先生)との共同研究グループは、脳波の自動判読法を開発し、その改良を続けていて、そのメンバーとして共同研究に参加しています。
2)高次脳機能と病態下の機能変容(可塑性)の解明
難治部分てんかんの外科治療には、てんかん焦点の切除と同時に焦点周囲の脳機能の温存が重要です。そのため、個々の病態による機能可塑性を加味しつつ、患者毎(テーラーメード)に、複合的なアプローチを用いた「システム」としての包括的な脳機能マッピングが必要とされます。我々は種々のマッピング手法を相補的に用いることで、病態下の高次運動・言語といった高次機能のマッピング手法の開発を試み、臨床応用してきました。臨床システム神経科学の観点からは、あくまで侵襲的な術前評価に限られますが、脳機能マッピングの中核検査と位置づけられる高頻度皮質電気刺激の手法は、非侵襲的な脳機能画像や疾病研究では得られない知見をもたらします。脳機能画像をもちいた賦活研究では特定の脳機能にかかわる皮質領野が可視化されますが、その領域が特定の脳機能発現に「必須」であるか見極めることが困難です。また、疾病(病巣)研究では、一般に脳機能可塑性(代償機構)がみられた慢性期に評価が行われますが、皮質電気刺激の手法では、刺激による効果は一過性(~5秒)で限局性(~1cm)であり、刺激介入時の課題の遂行障害の有無を評価することで、特定の高次脳機能の遂行に「必須」の皮質を同定することが可能です。
高頻度皮質電気刺激は、てんかん焦点の周囲の易興奮性を示す部位では、刺激電極や周囲の電極に棘波様の律動性放電(後発射)が出現して検査が困難となること、また実際にてんかん発作の誘発がまれに経験されます。Wideband EEGの特性を活かして、運動・高次機能などの課題中の神経活動を、運動準備電位・事象関連電位・高周波活動・律動(オシレーション)と皮質電気刺激とを相補的に用いることで包括的な皮質機能マッピングが可能となってきました。我々は、高頻度電気刺激で同定された側頭葉底面の言語領域において、意味処理課題中に事象関連電位が記録され、刺激介入で意味性錯語、反応時間の延長が出現することから、側頭葉底面言語野が言語機能の中で特に意味記憶(意味認知)にかかわることを示しました(図3)(Shimotake et al., 2014)。また、これらの側頭葉底面言語野、その周囲の高頻度電気刺激がおかしみ(mirth)、実際の笑いを惹起しうることからユーモアの意味理解にかかわることも明らかにしました。
さらに、我々は、皮質機能マッピングに加え、皮質-皮質間誘発電位(CCEP)の手法を用いて機能領野間の機能的結合を計測し、システム一体としての脳機能マッピング(system mapping)の臨床普及をすすめています。例として、脳神経外科と共同研究で、背側言語経路を担う弓状束の機能モニタリングに本手法を臨床応用しています。術前の解剖・機能的MRIおよびCCEPによる皮質間結合様式からブローカ野を同定したうえで、弓状束近傍の脳腫瘍切除術中にブローカ野を単発刺激し、後方言語野から記録されるCCEPを弓状束の結合性の動的指標としてモニタリングすることで弓状束の温存を図っています(本研究はHuman Brain Mapping誌に掲載されEditorʼs Choice Award 2014を受賞)。また、個々の患者から得られた各種皮質機能・ネットワークをその生理的・病的状態での変容も含めて、総合的に解析することで臨床システム神経科学への還元を目指しています。一例として一次体性感覚野で記録されるCCEPと体性誘発感覚電位に関連した高周波律動帯域の比較から、高周波活動の周波数は、水平・垂直伝播といった入力様式および入力する皮質層により規定されることを明らかにしました(Kobayashi et al. 2015)。
上記を含め、我々は侵襲的検査と非侵襲的検査(機能的MRI、diffusion tractography、MEG)を複合的に用いて、運動の中枢制御機構(葛藤制御・行為・到達運動・陰性運動現象)、言語機能(背側・腹側言語ネットワーク、意味認知)、視覚機能(retinotopic mapping)の解明および病態下のシステムレベルでの変容を明らかにしてきました。各種の課題が引き起こす複雑な神経活動に対しては本学内外の研究者と共同研究を行ってデコーディングも行っており(本学情報学部:辻本悟史先生、情報通信研研究機構:大須理英子先生、マンチェスター大学心理科学部:Lambon-Ralph先生)、今後は新学術領域のニューロオシロロジー(生理学研究所:南部篤教授)研究班の一翼(池田班)として正常脳機能およびてんかん病態のオシレーションの解明をさらに進める予定です。
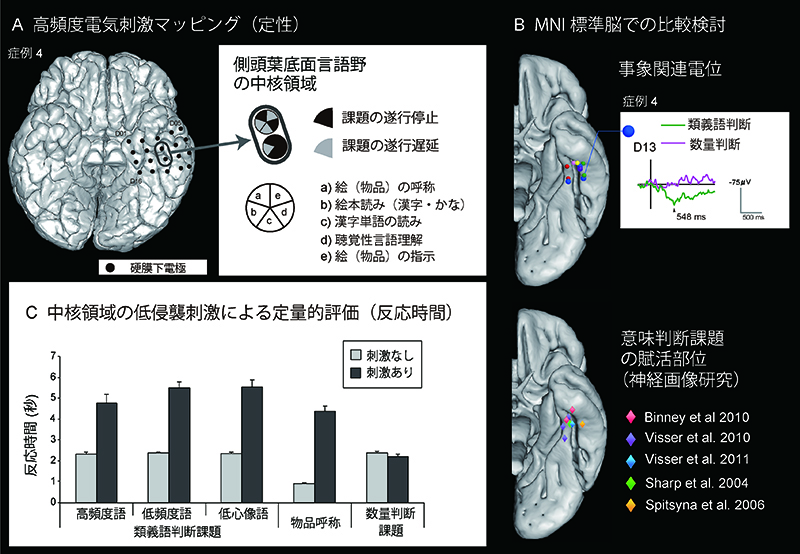
図3 硬膜下電極を用いた各種言語機能マッピング(代表例)
A. 従来の定性的な高頻度皮質電気刺激マッピング
左側頭葉底面に留置された電極から、各種言語課題遂行中に高頻度皮質電気刺激を行い、課題の遂行の停止・遅延の有無を検討した。楕円で囲まれた領域は、高頻度電気刺激・事象関連電位記録から同定された、側頭葉底面言語野の中核領域。
B. 上段のMNI標準脳には、6例の患者(個々の色)の側頭葉底面言語野の中核領域を提示。下段の健常者での各種意味判断課題を用いた神経画像研究の賦活部位と合致する。症例4での事象関連電位の代表波形を提示。類義語判断課題(意味記憶へのアクセス要)で、対照課題の数量判断課題に比して、明らかに大きな電位が記録された。
c. 低侵襲電気刺激による定量的評価(症例4)
より低侵襲の電気刺激を課題提示に時間を合わせて加えることで、各課題で反応時間を計測した。意味処理が必要な課題(類義語判断課題・物品呼称)では、刺激介入により有意に反応時間が延長した。一方、意味記憶へのアクセスが必要でない、対照の数量判断課題では刺激介入による反応時間延長はみられなかった。
Shimotake et al., 2014 より許可を得て改変引用。
3)運動異常症の病態解明と治療
様々な運動異常症の臨床および神経生理学的手法を用いた臨床研究を行っており、ミオクローヌスおよびミオクローヌスてんかんを来たす疾患を主な対象としています。良性成人型家族性ミオクローヌスてんかん(Benign adult familial myoclonus epilepsy: BAFME)は、約20年前から本邦および欧州から報告されている、①成人発症、②常染色体優性遺伝(原因遺伝子不明)、③皮質振戦(振戦様ミオクローヌス)、④稀発全般てんかん発作、⑤電気生理学検査で皮質反射性ミオクローヌスを呈する、を主徴とする疾患です。我々のグループは、その疾患概念の創生期より本疾患の臨床研究を行ってきました。BAFMEはその名の通り良性とされていましたが、加齢にともない皮質振戦が徐々に進行することが明らかになってきました。近年、我々は一次感覚運動野の興奮性の指標である体性感覚誘発電位の振幅が、BAFME患者では健常者に比して加齢にともない更に増大することを示し、BAFMEが緩徐進行性であることを病態生理学的に明らかにしました。またBAFMEにおいて世代を経るごとに、皮質振戦、稀発全般てんかん発作の発症年齢が低年齢化もしくはこれらの症状が新たに出現し、その傾向は母親から子に遺伝する際により顕著であることを示しました。この知見は、未知のBAFME原因遺伝子検索の一助となることが期待されています(東京大学辻省次先生)。また専門医へのアンケートを全国規模で行い、BAFMEが地域集積性のない全国に分布する疾患であることを明らかにしました(図4右)。
ウンフェルリヒト・ルンドボルク病(Unverricht-Lundborg disease: ULD)は、進行性ミオクローヌスてんかん(progressive myoclonus epilepsy: PME)の中核となる疾患であり、てんかん、ミオクローヌス、小脳失調、認知機能低下を主症状とし、欧州から主として報告されてきました。我々は本邦でもULDが存在することを報告し、これまでその名の通り進行性と考えられていたULDにおいて、進行が緩徐もしくは停止し、かつ皮質興奮性の指標である体性感覚誘発電位の振幅もほぼ一定で増加しない症例があることを示しました(図5)(Kobayashi et al., 2014)。また専門医へのアンケートを全国規模で行い、ULDを含めたPMEもBAFMEと同様に地域集積性がなく全国に分布する疾患であることを明らかにしました(図4左)。
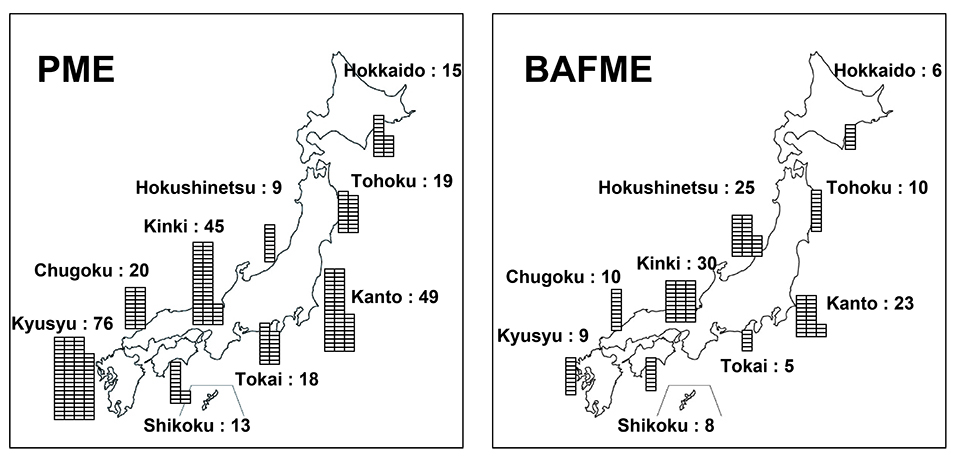
図4
アンケートによるBAFME患者(右)とPME患者(左)の日本国内の分布および症例数:BAFME・PME(ULD含む)患者は共に明らかな地域集積性がなく全国にまんべんなく分布していました。

図5
ULD患者(黒)と健常者(灰色)との体性感覚誘発電位の振幅と年齢の関係:健常者では加齢にともない体性感覚誘発電位の振幅は増大しますが、ULD患者では皮質興奮性の指標であるP25、N35成分の経時変化の程度(を示す回帰曲線の傾き)は健常者よりも大きくない、すなわち加齢に伴って皮質興奮性が異常に増大するわけではないことを示しています。Kobayashi et al., 2014より引用。
共同研究者一覧
支援講座および運営委員会構成講座とは常時共同研究をいたしております。
それ以外の共同研究者を提示しています。
[海外](アルファベット順に記載)
Dr. Stéphanie Baulac, Ph.D.
所属: Institut du Cerveau et de la Moelle épinière (ICM), Epilepsy Unit
役職: Research Director
Dr. Christophe Bernard, Ph.D.
所属: INS – Institut de Neurosciences des Systèmes, UMR INSERM 1106, Aix-Marseille Université
役職: Team leader
Dr. Marco Catani, M.D., Ph.D.
所属: Natbrain lab, Department of Forensic and Neurod evelopmental Sciences, Institute of Psychiatry,
Kingʼs College London
役職: Clinical Senior Lecturer and Honorary Consultant Psychiatrist
Prof. Nathan Earl Crone, M.D.
所属: Department of Neurology, Johns Hopkins University School of Medicine
役職: Professor
Dr. Marco De Curtis, M.D.
所属:Fondazione IRCCS Istituto Neurologico Carlo Besta
役職:Head of Epileptology and Experimental Neurophysiology Unit, Head of Pre-clinical Neuroscience Laboratories
Prof. Mattew A. Lambon-Ralph, FRSLT (hons), FBPsS
所属: School of Psychological Sciences, University of Manchester
役職: Professor of Cognitive Neuroscience & Associate Vice-President (Research)
Dr. Dileep R. Nair, M.D.
所属: Epilepsy Center, Cleveland Clinic
役職: The Section Head of Adult Epilepsy and Director of Intraoperative Neurophysiologic monitoring
Prof. Angela Vincent, Ph.D.
所属: University of Oxford
役職: Emeritus professor
[国内](五十音順に記載)
飯田幸治先生
所属:広島大学医学部附属病院脳神経外科
役職:講師
井上有史先生
所属:国立病院機構静岡てんかん・神経医療センター
役職:院長
今水 寛先生
所属:東京大学大学院人文社会系研究科心理学研究室
役職:教授
大須理英子先生
所属:脳情報通信総合研究所,国際電気通信基礎技術研究所
役職:研究室長
大沼悌一先生
所属:むさしの国分寺クリニック
役職:名誉院長
加藤天美先生
所属:近畿大学医学部附属病院脳神経外科
役職:主任教授
亀山茂樹先生
所属:国立病院機構西新潟中央病院
役職:名誉院長
齋藤 智先生
所属:京都大学大学院教育学研究科教育認知心理学講座
役職:准教授
柴崎 浩先生
京都大学名誉教授(神経内科)
杉 剛直先生
所属:佐賀大学海洋エネルギー研究センター
役職:准教授
辻 省次先生
所属:東京大学医学部附属病院神経内科
役職:教授
辻本悟史先生
所属:京都大学情報学研究科知能情報学専攻生命情報学講座
役職:准教授
内藤 栄一先生
所属:情報通信研究機構(NICT)脳情報通信融合研究センター
役職:研究マネージャー
中村政俊先生
所属:佐賀大学先端研究教育施設システム制御研究所
役職:名誉教授
長峯 隆先生
所属:札幌医科大学神経科学講座
役職:教授
西田茂人先生
所属:福岡工業大学情報工学部情報通信工学科
役職:教授
矢野育子先生
所属:京都大学医学部附属病院薬剤部
役職:副薬剤部長・准教授
山本洋紀先生
所属:京都大学大学院人間・環境学研究科
役職:助教











